原子,这个构成物质世界的基本单元,其结构一直是科学研究的重要领域,了解原子的结构模型及组成,对于我们理解物质的性质和化学反应的本质具有至关重要的意义。
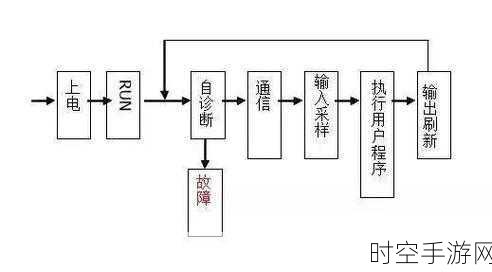
原子结构模型经历了漫长的发展历程,从早期的道尔顿模型,到汤姆逊的“葡萄干布丁”模型,再到卢瑟福的核式结构模型,以及后来的玻尔模型和现代量子力学模型,每一次的进步都让我们对原子的认识更加深入。

原子由原子核和核外电子组成,原子核位于原子的中心,由质子和中子构成,质子带正电荷,中子不带电,核外电子围绕原子核做高速运动,电子带负电荷,原子中质子数等于电子数,因此整个原子呈电中性。
要深入理解原子结构,还需要掌握一些关键概念,比如原子半径,它分为共价半径、金属半径和范德华半径等,不同元素的原子半径大小不同,并且会受到原子序数、电子层数和核电荷数等因素的影响。
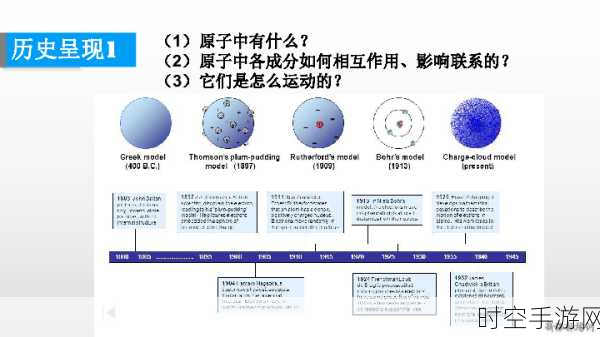
电子的排布遵循一定的规律,根据能量最低原理、泡利不相容原理和洪特规则,电子会按照特定的顺序填充不同的能级和轨道。
在研究原子结构的过程中,科学家们运用了多种实验手段和理论方法,通过 X 射线衍射实验可以确定晶体中原子的排列方式,从而间接推断原子的结构;利用光谱分析可以研究原子的能级和电子跃迁情况。
原子结构是一个复杂而又充满魅力的领域,通过不断地探索和研究,我们能够更加深入地了解物质的本质,为新材料的研发和新技术的应用提供坚实的理论基础。
参考来源:《化学基础教程》《原子物理学》等相关教材和学术著作。